副作用の少ない抗がん剤の開発に成功
― 4本鎖DNAを標的とした新しい抗がん剤 ―
九州工業大学大学院工学研究院の竹中繁織教授、佐藤しのぶ准教授、Tingting Zou助教(現在、住友ファーマ研究員)、同大大学院情報工学研究院の藤井 聡助教、九州歯科大学口腔応用薬理学分野の竹内 弘教授、福田 晃助教らの研究グループは、副作用の低い抗癌剤を新たに開発しました。
ポイント
- 生体内の4本鎖DNA(G4)構造に特異的に結合する分子としてcAQ-mBenを開発した
- 遺伝子発現量解析の結果、AQ-mBenはがん関連の遺伝子群に影響を与え、がん細胞を細胞死に誘導することを明らかにした
- cAQ-mBenを担癌マウスに投与したところ、広く使用されている既存の抗がん剤と同程度の抗がん作用を示したが、腎機能、肝機能への影響はほとんどなかった(副作用なし)
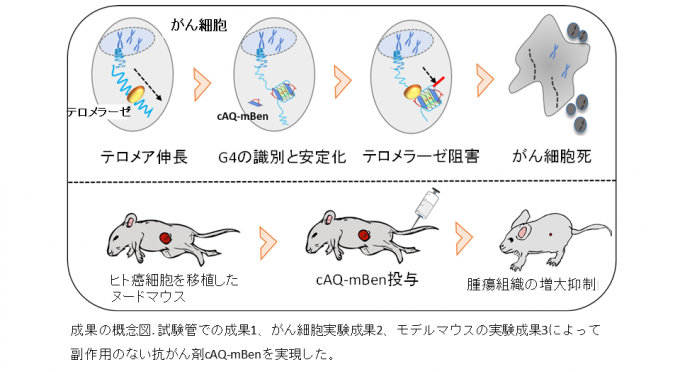
本研究グループは、副作用の少ない抗がん剤となりうる分子を開発しました。がん治療で用いられている従来の抗がん剤(例えばシスプラチン)は、がん細胞だけではなく、正常細胞にも作用して、副作用を引き起こします。そのため、がん細胞に選択的に働く薬の登場が強く望まれています。ほとんどのがん細胞は、テロメラーゼという酵素の発現によって染色体末端のテロメアDNAが伸長することで不死化します。 注1) テロメアDNAは4本鎖DNA(G4)を形成することが明らかになってきており、 注2) この構造を安定化すると、テロメラーゼがテロメアDNAを伸長できず、がん細胞の細胞死が誘導されることから、新しい抗がん剤の標的として注目されています。本研究グループは副作用軽減のため、通常の2本鎖DNAには結合せず、G4に結合する分子として、様々な環状アントラキノン(cAQ)誘導体を開発し、そのうちcAQ-mBenがG4に強く結合することを明らかにしました。また、遺伝子発現量解析 注3) の結果、cAQ-mBenはがん関連の遺伝子やがん抑制に関連する経路に影響を与え、アポトーシス(細胞の自己崩壊)を引き起こしている可能性が示唆されました。さらに、cAQ-mBenが影響を与える遺伝子には、G4構造を形成しやすい配列が多く存在していたことから、cAQ-mBenがG4に結合して遺伝子の制御を行っていることが予想されました。担がんマウスにcAQ-mBenを投与したところ、既存の抗がん剤シスプラチンと同じくらい効果的にがんの成長を抑制しましたが、マウスの腎機能、肝機能にはほとんど影響を与えませんでした。すなわち、cAQ-mBenによって副作用のない抗がん剤の道を開きました。
本研究成果は、2023年6月24日に米国科学アカデミー発行の国際科学雑誌「PNAS Nexus」のオンライン版で公開されました。研究の詳細は別紙をご参照ください。
【研究概要】
がんは、20年以上も我が国の死亡率の第一位を占めている。がん治療として手術、放射線治療、薬物治療が行われてきた。従来の抗がん剤に加え分子標的薬の登場によって治療成績が飛躍的な進歩を遂げている。しかし、治癒することは稀で、がんを抱えながら生活する時間が長くなっている。抗がん剤の投与期間が長くなるため副作用の低い抗がん剤が望まれている。最近、テロメラーゼをターゲットとした抗がん剤の開発が注目されている。テロメラーゼは染色末端に存在するテロメアDNAを伸長する酵素でがん細胞の不死化に係っている。すなわち、テロメラーゼのターゲットであるテロメアDNAへのアクセスを阻害できる薬剤は副作用の低い抗がん剤として期待される。テロメアDNAはG4構造を形成することが知られてきた。従って、その構造を特異的に安定化できる分子は、副作用のない抗がん剤として発展できる可能性がある。この観点からG4特異的安定化分子の開発が世界中で行われている。九州工業大学と九州歯科大学との研究グループは、環状アントラキノン誘導体(cAQ-mBen)と呼ばれる分子を開発し、これが副作用の低い抗がん剤となりうることを示した。
成果1:cAQ-mBen分子を設計?合成する方法を開発した。cAQ-mBenはG4 DNA特異的に結合して、その構造を安定化できることを明らかにした。また、がん細胞中のG4 DNAへ結合していることを細胞の蛍光イメージングで証明した。さらに、テロメラーゼを特異的に阻害することも明らかにした。正常細胞に影響を与えずにがん細胞のみの生育を効果的に阻害することを明らかにした。
成果2:細胞で働いているすべての遺伝子群のRNA-Seqによる網羅的解析とバイオイフォマッテクスの手法によって、cAQ-mBenはがん関連の遺伝子やがん抑制に関連する経路に影響を与えること、ミトコンドリア内の酸化的リン酸化(OXPHOS)関連遺伝子群を抑制することが明らかとなった。このことは、cAQ-mBenがアポトーシスを引き起こしていることが示唆された。さらに、cAQ-mBenが影響を与える遺伝子群のプロモーター領域や遺伝子上には、G4構造を形成する可能性のある配列が多く存在していることがわかった。このことから、cAQ-mBenがG4に結合して遺伝子の制御を行っていることが示唆されました。
成果3:ヒト由来癌細胞を植え付けたヌードマウス(マウス異種移植モデル)における抗腫瘍活性に関して、cAQ-mBenはシスプラチンと同等の腫瘍抑制効果を示した。シスプラチン投与マウスでは病理組織学的検査および血清生化学的検査において肝臓、腎臓、精巣に重篤な副作用が現れ、体重も減少したが、cAQ-mBenを投与しても、これらの副作用は見られなかった。
以上の結果から、分子設計のよって合成されたcAQ-mBenは副作用のない効果的な抗ガン剤として発展できる可能性を示すことができた。
【発表雑誌】
| 論文タイトル | “Cyclic anthraquinone derivatives, unique G-quadruplex binders, selectively induce cancer cell apoptosis and inhibit tumor growth” |
| 著者 | Hikaru Fukuda, Tingting Zou, Satoshi Fujii, Shinobu Sato, Daiki Wakahara, Sen Higashi, Ting-Yuan Tseng, Ta-Chau Chang, Naomi Yada, Kou Matsuo, Manabu Habu, Kazuhiro Tominaga, Hiroshi Takeuchi, Shigeori Takenaka |
| 雑誌名 | PNAS nexus Published: 23 June 2023 |
| DOI | https://doi.org/10.1093/pnasnexus/pgad211 |
※ 本研究はJSPS科研費JP19K15700,JP18K09775,JP22K17164, JP19H02748の助成を受けたものです。
用語解説
注1) テロメアDNAとテロメラーゼ:
生物の染色体末端に見られる繰り返し配列をテロメアと呼ばれている。ヒトの場合はTTAGGGの繰り返し配列である。テロメラーゼは成熟した細胞では存在しないが、がん化によって発現するようになる。このことからがんの不死化に必修であるとともに抗がん剤のターゲットにもなっている。
注2) 4本鎖(G4)DNA:
ヒトテロメアのようにTTAGGGが4回繰り返すと折り畳まれて4本鎖を形成する。この際、グアニン(G)が水素結合によってG-カルテット平面を形成し、これが積み重なって形成される。
注3) 遺伝子発現量解析:
次世代シークエンサーの発展によって細胞で働いているすべてのmRNAを解析できるようになった。がん細胞と正常細胞で発現しているmRNAの違いを調べればがんに関係する遺伝子を調べることができる。ここではcAQ-mBen添加によってがん細胞の遺伝子群がどのような変化をしているかを見ることができる。
【研究内容に関するお問い合わせ】
九州工業大学 大学院工学研究院物質工学研究系 教授 竹中 繁織
TEL: 093-884-3322
E-mail: shige*che.kyutech.ac.jp
九州歯科大学 健康増進学講座 口腔応用薬理学分野
TEL: 093-285-3053
E-mail: r12takeuchi*fa.kyu-dent.ac.jp
【報道に関するお問い合わせ】
九州工業大学 総務課 広報係
TEL: 093-884-3007
E-mail: pr-kouhou*jimu.kyutech.ac.jp
(メールは*を@に変えてお送りください)